
Próxima remessa do imunizante para o Ministério da Saúde está prevista para 13 dias. Governo de São Paulo alerta sobre a necessidade de ampliar a oferta de fármacos contra a covid. Fiocruz prevê repasse de 4,7 milhões de doses esta semana

Ainda refém da importação de insumos para a produção de vacinas contra a covid-19 em território nacional, o Brasil está sob risco de uma nova desaceleração no ritmo de vacinação dos brasileiros. Nesta segunda-feira (19/4), o principal fabricante do fármaco contra a covid-19, o Instituto Butantan, entregou ontem 700 mil doses da CoronaVac ao Ministério da Saúde. O próximo repasse está previsto para 13 dias, após o processamento de 3 mil litros de insumos que chegaram da China nesta segunda-feira. O Butantan prevê a entrega de 5 milhões de doses em 3 de maio. Até lá, caberá à Fundação Oswaldo Cruz abastecer o Programa Nacional de Imunização.
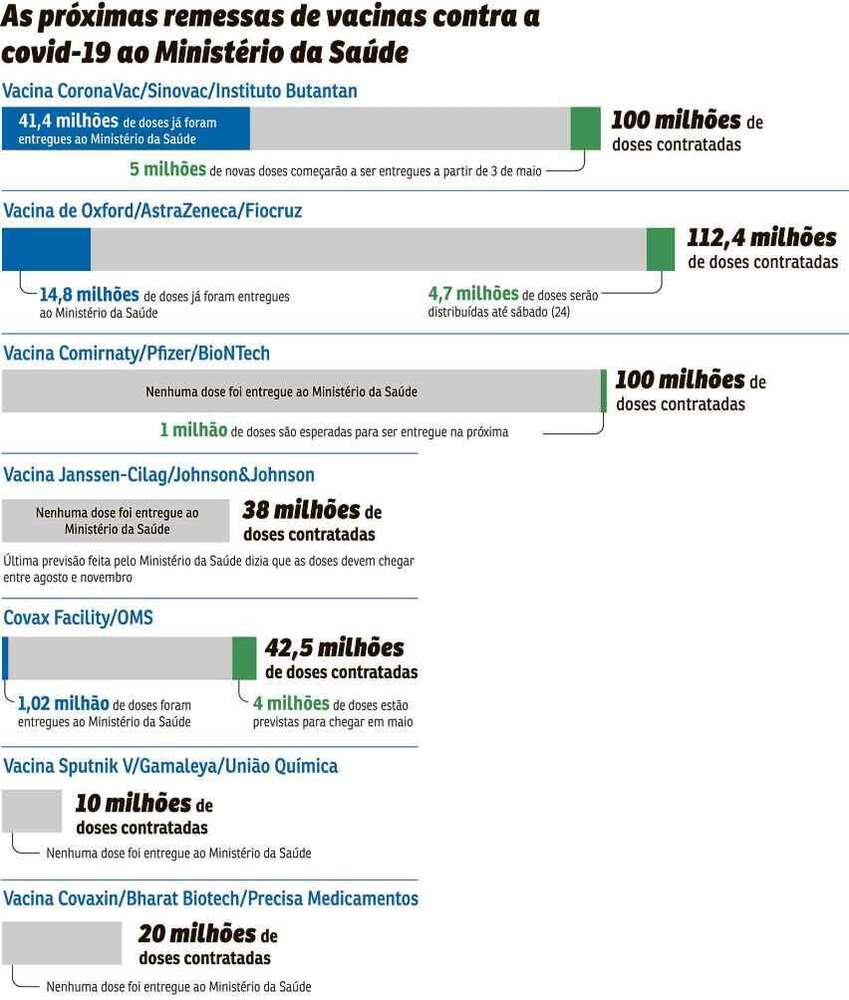
O lote de 700 mil unidades da CoronaVac entregue pelo Butantan é o último repasse previsto para abril, em razão dos atrasos na chegada da matéria-prima proveniente da China. Com o repasse de ontem, o Butantan totaliza 41,4 milhões de doses disponibilizadas ao governo federal. No contrato firmado com o Ministério da Saúde estava prevista a entrega de 46 milhões de unidades até o fim de abril, mas questões burocráticas atrasaram a chegada do insumo farmacêutico ativo (IFA). Por conseguinte, as 4,6 milhões de doses faltantes somente estarão disponíveis em maio.
“De fato, houve atraso (no recebimento do IFA) de mais de 10 dias. A burocracia é uma dificuldade, e nós estamos trabalhando no sentido de vencer isso. Existe uma demanda muito grande de vacinas do mundo todo a partir da China, e isso tem redundado nesses atrasos. Estamos fazendo todo esforço para acelerar a produção (…) para que essas vacinas sejam entregues o mais rapidamente possível. A partir do dia 3 de maio, nós voltamos a entregar vacinas”, confirmou o diretor do Instituto Butantan, Dimas Covas, em coletiva de imprensa.
O governador de São Paulo, João Doria, reconheceu o atraso e voltou a ressaltar a necessidade da chegada de outros imunizantes. “A partir do dia 3 de maio, com os insumos que chegaram hoje (ontem), nós estaremos entregando a vacina do Butantan para o Ministério da Saúde. Portanto, temos aí três dias de atraso. Esperamos também que não só a AstraZeneca, com a Fiocruz, como também outras vacinas adquiridas e prometidas pelo governo federal possam ser entregues para a vacinação dos brasileiros ”, disse.
A maior parte das vacinas aplicadas nos brasileiros até o momento é do instituto paulista. “De cada 10 brasileiros que tomam a vacina no braço, oito tomam a vacina do Butantan”, ressaltou Doria. Para as próximas semanas, por enquanto, o instituto só tem garantido a produção de mais 5 milhões de vacinas a partir do IFA recebido ontem. Um outro lote de 3 mil litros de insumo também aguarda autorização para ser importado da China.
Com essa pausa nas entregas feita pelo Butantan, a Fiocruz é quem vai sustentar um ritmo de vacinação com a entrega de doses da vacina de Oxford/AstraZeneca ao longo desta e da próxima semana. A produção de abril e maio está garantida com os lotes de IFA recebidos até o momento. Com isso, novas 4,7 milhões de unidades serão disponibilizadas ao PNI ainda nesta semana. A entrega será parcelada: uma parte das doses será enviada amanhã, a outra, na sexta. Na próxima semana, a Fiocruz disponibiliza a maior quantidade de vacinas do mês de abril: 6,7 milhões de doses.
Reação à AstraZeneca
Além da escassez de vacinas, motivo para a lentidão no processo de imunização dos brasileiros, os gestores lidam com uma desconfiança em relação ao fármaco produzido pela Fiocruz. De acordo com o governo do Distrito Federal, idosos deixaram de vacinar por medo da vacina da AstraZeneca. “Hoje temos duas vacinas disponíveis aqui no DF, Coronavac e AstraZeneca. Na última remessa, veio quase que integralmente de Astrazeneca, e percebemos que parte da população tem resistência de tomar essa vacina”, disse o secretário da Casa Civil do DF, Gustavo Rocha, ontem, durante coletiva de imprensa.
O secretário de Saúde Osnei Okumoto indicou que, até o momento, o DF registrou apenas 1.445 efeitos adversos às vacinas, sendo 500 de AstraZeneca. No início do mês de abril, a Agência Nacional de Vigilância Sanitária (Anvisa) incluiu “possíveis ocorrências tromboembólicas com trombocitopenia” no item “Advertência e Precauções” da bula da vacina de Oxford/Astrazeneca.
Segundo a Anvisa, no Brasil, até o momento, foram registrados 47 casos suspeitos de eventos adversos tromboembólicos com pessoas imunizadas com a vacina de Oxford/AstraZeneca, no entanto, a Anvisa esclarece que, até o momento, não foi possível estabelecer uma relação direta e de causalidade entre esses casos com o uso do imunizante.
A Fiocruz publicou nota no próprio site reforçando que o risco de trombose pela infecção por covid-19 é maior do que por vacinas. “Um estudo estudo de pesquisadores da Universidade de Oxford indica que o risco de ocorrer trombose venosa cerebral em pessoas com covid-19 é consideravelmente maior do que nas que receberam vacinas baseadas na tecnologia de RNA mensageiro (mRNA), como os imunizantes da Pfizer, Moderna e Oxford/AstraZeneca, produzida no Brasil pela Fundação Oswaldo Cruz (Fiocruz)”, disse a entidade.
Teste com imunizante
Em busca de novas vacinas para combater o novo coronavírus, a Agência Nacional de Vigilância Sanitária (Anvisa) aprovou a realização de um novo ensaio clínico de imunizante contra a covid-19 no Brasil. Os testes em humanos da vacina da empresa Sichuan Clover Biopharmaceuticals, sediada na China, serão realizados no país com 12.100 voluntários, a partir de 18 anos de idade, distribuídos entre Rio Grande do Sul, Rio Grande do Norte e Rio de Janeiro.
O imunizante testado também funciona no sistema de duas doses, como a maioria dos já utilizados no mundo. Cada voluntário receberá duas aplicações, com intervalo de 22 dias entre elas. A empresa realizará no Brasil estudos de fase 2 e 3, nos quais são avaliadas a segurança da vacina, imunogenicidade e eficácia do imunizante. Segundo a Anvisa, o início dos testes em seres humanos depende de dois fatores.
Um deles é a aprovação no Conselho Nacional de Ética em Pesquisa (Conep), órgão do Ministério da Saúde responsável pela avaliação ética de pesquisas clínicas. Outro fator que determina o início dos testes é a organização interna dos pesquisadores para o recrutamento dos voluntários. “O prazo para início do estudo clínico após a aprovação ética e regulatória é definido pelo patrocinador dos teste”, informa a Anvisa.
Ao todo, 22 mil voluntários partiparão dos estudos da vacina da Sichuan Clover, que ocorrem em outros países como China, Bélgica e África do Sul. Para autorizar a realização dos testes em brasileiros, a agência reguladora analisou dados de etapas anteriores do desenvolvimento da vacina, incluindo estudos não clínicos in vitro e em animais. “Os resultados obtidos até o momento demonstraram um perfil de segurança aceitável das vacinas candidatas”, diz a nota da agência.
Esse é o sexto estudo de vacina contra a covid-19 autorizado pela Anvisa. Já foram realizados testes da vacina de Oxford/AstraZeneca, da CoronaVac, da vacina Comirnaty, da Pfizer, do imunizante da Janssen-Cilag e, mais recentemente, do imunizante desenvolvido pela empresa canadense Medicago R&D. Todas as vacinas, tirando a da Medicago, já foram compradas pelo governo federal, uma vez que a Anvisa também autorizou o uso emergencial ou concedeu o registro aos imunizantes após os testes de fase 2 e 3.